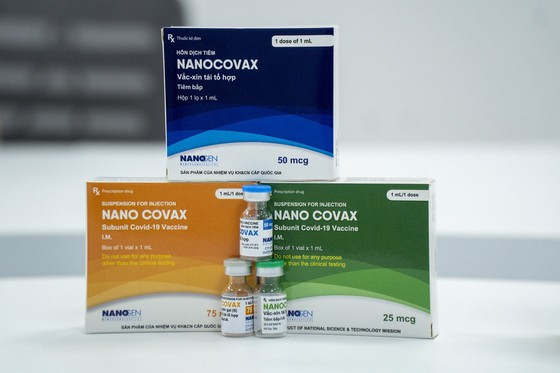
[인사이드비나=하노이, 떤 풍(Tan phung) 기자] 베트남이 자체개발한 코로나19 백신인 나노코백스(Nanocovax)가 긴급사용 승인까지 한걸음을 남기고 추가자료 제출이 요구됐다.
보건부 산하 의약품 및 의약품원료 허가 자문위원회(이하 자문위)는 29일 저녁 회의 직후, 개발사인 나노젠(Nanogen)에 나노코백스 임상시험 관련 추가자료 제출을 요구하며 긴급사용 승인을 보류했다.
자문위는 보도자료를 통해 “나노젠이 제출한 나노코백스 서류를 법률, 품질, 약리학, 임상기록 및 국가윤리위원회의 결론을 기반으로 여러번 신중하게 검토 및 평가한 결과 자료 보완을 요구했다"고 밝혔다.
자문위가 요구한 추가자료는 백신의 품질서류, 임상 및 약리학적 서류, 최소 1회접종자에 대한 안정성 보완자료 및 심각한 부작용(SAE) 사례, 변이바이러스(알파, 델타 등)에 대한 면역원성 평가자료, 임상시험 대상자 크기 등이다.
자문위는 나노젠에 추가자료를 신속히 보완해 제출할 것을 권고하며, 추가자료에 하자가 없을 경우 즉시 보건부에 긴급사용 승인을 요청할 것이라고 밝혔다.
28일 간격으로 2회 접종하는 나노코백스는 임상시험 및 긴급사용 승인을 신속히 진행하기 위해 임상3a 중간결과만으로 지난 6월말 긴급사용 신청됐다. 임상3a에는 1000명을 대상으로 연구가 진행됐으며 최종결과는 내달 10일 나올 것으로 예상된다. 현재 1만2000여명을 대상으로 진행중인 임상3b상의 최종결과는 내년 2월까지가 목표다.
이에따라 나노코백스의 긴급사용 승인은 임상3a 최종결과가 나오는 내달 10일 이후에나 가능할 것으로 예상된다.